白 晨* 梁 波 王淑珍1 郑小迅 林志平2 黄伟达
(复旦大学生物化学系,上海200433;1上海师范大学生物系,上海200234;2复旦大学化学系,上海200433)
氨基糖广泛存在于抗生素、海洋天然药物等多种通过特殊代谢途径产生的生物活性化合物中。最近一些研究表明,微生物的代谢产物中存在非常见的L2型糖[1,2],并且非天然L2型合成糖苷类药物对某些病毒具有选择性杀伤作用[3],糖类D、L2构型是新型糖类药物研究中的重要内容。但在新种类氨基糖苷类化合物的初期研究中,往往由于其存在量少、提取纯化困难,很难应用常规的旋光度法分析所含糖类的D、L构型。而现有的以(-)22丁醇,(+)222辛醇[4,5]、二[(+)212苯乙基]二硫缩醛[6]、L2半胱氨酸甲酯盐酸盐[7]等为手性衍生化试剂的单糖D、L构型气2液层析分析方法,虽然部分可以用于氨基糖[3],但由于在这些方法中手性试剂的标识反应是通过糖醛基与试剂的羟基或氨基的缩合反应完成的,使得反应得率低、操作烦琐、糖由来的副反应生成物较多。同时也导致了分析灵敏度只能停留在微摩尔水平。因此具有更高灵敏度的氨基糖D、L构型新分析方法的开发十分必要。近年来,荧光手性试剂的研究开发发展迅速,已成为化合物立体构型分析研究中的重要内容之一。手性荧光试剂(S)2(+)222叔丁基222甲基2苯并1,32二氧杂环戊烷242甲酸[(S)2(+)2TBMB甲酸]曾被用于中性糖的D、L2构型分析[8,9],其糖衍生物的激发波长为310nm,荧光波长为380nm,分析灵敏度达到pmol水平。本文中我们将(S)2TBMB甲酸转变为其酰氯[10],使其与氨基糖专一选择性反应,再经完全乙酰基化,将氨基糖D、L对映体转变为非对映的极性较低的糖衍生物。利用氨基糖衍生物1HNMR图谱中叔丁基及甲基特征信号峰的D、L体间的化学位移差异,分析了对应氨基糖的D、L构型。其后又结合反相HPLC,创立了适合于痕量氨基糖的D、L构型分析的更为简便的高灵敏度新方法,并根据上述方法对天然及合成得到的已知D、L构型的6种氨基糖作了分析比较。
1 材料和方法(MaterialsandMethods)
1.1 试剂与仪器
JEOLGSX2270MHz型核磁共振仪,室温,CDCl3溶剂,TMS内标;(S)2TBMB甲酸、(R,S)2TBMB甲酸[11]、3-氨基2-脱-2D-葡萄糖、4-氨基-4-脱氧-D-甲基葡萄糖苷、6-氨基-6-脱氧2D-葡萄糖[12,13]按文献方法制备,2-氨基2-脱氧-D-葡萄糖盐酸盐、2-氨基-2-脱氧-D-甘露糖、2-氨基-2-脱氧-D-半乳糖、N,N2二甲基甲酰胺、异丙醇、乙腈(HPLC用)、三乙基胺购于Sigma,其他试剂均为国产分析纯试剂。
1.2 方法
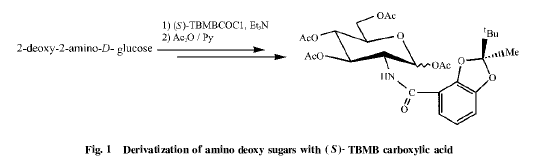
1.2.1 氨基糖的(S)2TBMB甲酸标记及完全乙酰基化反应(见图1) 在10ml体积的锥型试管中加入3mg氨基糖或其盐酸盐及500Ll甲醇,搅拌,待氨基糖完全溶解后加入20Ll三乙基胺,搅拌2~3min后,加入500Ll(S)2TBMB酰氯的二氯甲烷溶液[含35mg(S)2TBMB酰氯],搅拌10min后,将反应液真空浓缩。浓缩物中加入500Ll吡啶,100Ll醋酸酐,45bC反应30min。反应结束后加入
500Ll乙醇,500Ll甲苯搅拌5min,减压浓缩,浓缩物经薄层层析(甲苯B乙酸乙酯=2:1)纯化后得到完全乙酰基化氨基糖羧酸衍生物,用于1HNMR测
定。
1.2.2 HPLC分离分析氨基糖D、L2异构体 氨基糖的D、L2异构体分析在CCPM型HPLC装置,FS28010型荧光检测仪(Tosoh,Japan)上进行。层析柱为反相ODS柱(4.5mm<@150mm,Shise2do,Japan)。移动相溶液乙腈B水B异丙醇=4:4:1或乙腈B水B异丙醇=3B7B2(WBWBW),荧光检测波长Em:310nm,Ex:370nm。
2 结果和讨论(ResultsandDiscussion)
2.1 氨基糖的衍生化反应
糖的衍生化反应包括(S)2TBMB羧酸荧光标识反应及常规的完全乙酰基化反应两个部分。荧光标识反应中,(S)2TBMB甲酸被转化为其对应的酰氯(溶于二氯甲烷,保存在-20bC,3天内使用,不影响反应得率)在甲醇与三乙基胺的混合溶液中与氨基糖反应。这一反应中存在(S)2TBMB酰氯的加
水分解副反应。反应液pH值或溶液的含水量过高均会促进这一副反应的进行。因此,选用微量的三乙基胺为碱基催化剂,反应试剂均经分子筛(0.4
nm)干燥,并保存在真空干燥箱中。荧光标识反应结束后,反应液的浓缩物被直接用于第二步的完全乙酰基化反应。本研究中使用过量的TBMB荧光标识试剂,氨基糖的衍生化反应经薄层层析检测未见有其他副反应生成物。由于4-氨基吡喃糖极易发生分子内脱水反应,在中性乃至弱酸性条件下,生
成1,4-二脱氧21,42亚氨基糖醇[14],其合成及与(S)2TBMB酰氯的衍生化反应均十分困难。而结合于C4位的TBMB试剂与C1位距离较远,C1位基团对4-氨基糖D、L体分离影响较小。因此本研究选择了稳定的4-氨基-4-脱氧-D-甲基葡萄糖苷为4-氨基糖的分析模型分子。
2.2 完全乙酰基化D、L氨基糖的核磁共振分析
由于L2型氨基糖较难得到,本文与以往研究相同[8,9],利用(S)2TBMB甲酸与(R)2TBMB甲酸的消旋混合体与D型氨基糖反应,得到1B1的对应衍生物,其中(R)2TBMB甲酸的D-氨基糖衍生物被视为(S)2TBMB甲酸与L2氨基糖的衍生物。2-氨基-D-葡萄糖及合成得到的3,62氨基D-葡萄糖、4-氨基甲基-D-葡萄糖苷,经(S)及(R,S)消旋体TBMB甲酸荧光标识,完全乙酰基化得到对应的衍生物,被用于1HNMR分析。生成的氨基糖衍生物均包括A、B异头体,其中A异头体较多。在其1HNMR图谱中,叔丁基及甲基信号峰分别处于
1.1及1.6ppm附近的较高磁场,与其他信号峰无重叠。除B异头体的32氨基糖外,其他氨基糖衍生物的D、L体的叔丁基及甲基的化学位移均有不同
度的差异(表1)。
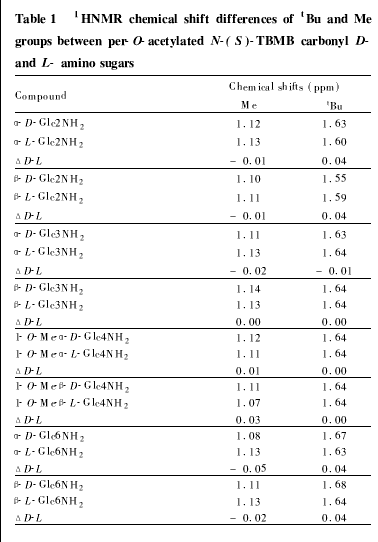
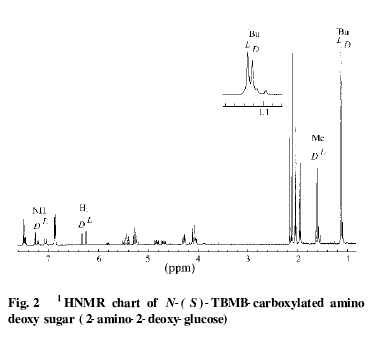
图2是一个典型的1HNMR图谱,在这图谱中22氨基葡萄糖D、L异构体的叔丁基、甲基、氨基及C1位连接的氢原子的信号峰均达到了很好的分离。
2.3 D,L2氨基糖的高灵敏度HPLC分析方法
氨基糖经荧光标识及完全乙酰基化后,生成物无需纯化,浓缩后的反应溶液经稀释后可直接用于HPLC分析。HPLC分析法的全部分析时间低于2
h,利用手性试剂(S)2TBMB的强荧光发光分析灵敏度可达到0.2pmol。具体操作:1Lg的氨基糖溶于50Ll甲醇,加入3Ll三乙基胺,(S)2TBMB酰氯的二氯甲烷溶液50Ll[含0.5mg(S)2TBMB酰氯],搅拌15min,反应液经浓缩后加入50Ll吡啶,10Ll醋酸酐,将生成物完全乙酰基化。反应结束后加入20Ll乙醇,真空浓缩,浓缩物经50LlHPLC移动相溶液稀释后,取2Ll用于HPLC分析。

本文利用反相ODS层析柱对6种氨基糖的DL体进行了分析比较、结果如图3所示。
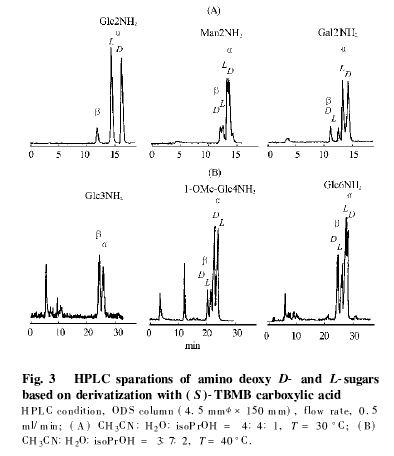
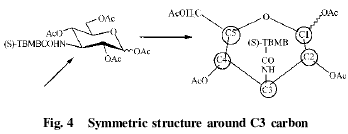
3种2-氨基糖的HPLC分析中,乙腈:水:异丙醇=4:4:1为最佳移动相配比,柱温为30度;3,4,62氨基葡萄糖的分析中,乙腈:水:异丙醇=3:7:2为最佳移动相配比,柱温为40度。HPLC分析结果表明除32氨基葡萄糖之外,其他5种氨基糖的D、L异构体均有不同程度的分离,其中22氨基葡萄糖的A异头体,22氨基半乳糖的A异头体,B异头体,42氨基甲基葡萄糖苷的A异头体,B异头体及62氨基葡萄糖的B异头体的D、L体分离度(Rs)大于或接近1.25。所有A2氨基糖衍生物的HPLC分析结果均是D体的保留时间长于L体,而B体则相反,呈现一定的规律性。我们尝试了多种HPLC移动相配比应用于32氨基葡萄糖,均未达到D、L体的分离。其原因可能是由于在糖衍生物中(S)2TBMB甲酸手性试剂处于相对对称的空间位置(图4),减小了手性试剂标识后D、L体间的结构差异。
相反在62氨基葡萄糖的分析中,虽然,由于6位碳原子为非手性碳原子,相对其他氨基糖,62氨基糖的手性中心与(S)2TBMB甲酸的手性中心距离较远,但可能由于其(S)2TBMB羧酸衍生物在空间构象上,手性试剂的手性中心与糖的手性碳原子较为接近,其D
、L体却得到了很好的分离结果。以上结果说明氨基糖的D
、L异构体(S)2TBMB羧酸衍生物的分离不仅依存手性试剂与糖的手性中心的结合距离,而且与(S)2TBMB甲酸结合后的空间位置有直接关系。
[
本帖最后由 fjdlgldg 于 2010-9-2 16:08 编辑 ]

