查看完整版本请点击这里:
【求助】请帮忙看看2-D图是过聚焦了还是聚焦不充分?
【求助】请帮忙看看2-D图是过聚焦了还是聚焦不充分?
请筒子们帮忙看看我跑的这块胶,植物样品,上样前1 mg蛋白用2-D cleanup,pH3-7,18 cm胶条,被动水化16 h。IEF聚焦程序:
S1 grad 60 v 3h
S2 grad 500 v 1 h
S3 grad 1000 v 1h
S4 grad 10,000 v 5 h
S5 step 10,000 v 40,000 vh
S6 step 2000 v 8h
总聚焦77,700 vh
1% DTT平衡13 min,3% Iodo平衡17 min。
第二向12%的胶,15°C,2w/gel 45 min,17w/gel 4 h。考染
我觉得这个图上的点还是不够圆和清晰,不知道是聚焦不够还是过聚焦了,不知还需要哪些改进,请大家帮忙看看,不胜感谢!
查看完整版本请点击这里:
【求助】请帮忙看看2-D图是过聚焦了还是聚焦不充分?
【求助】请帮忙看看2-D图是过聚焦了还是聚焦不充分?
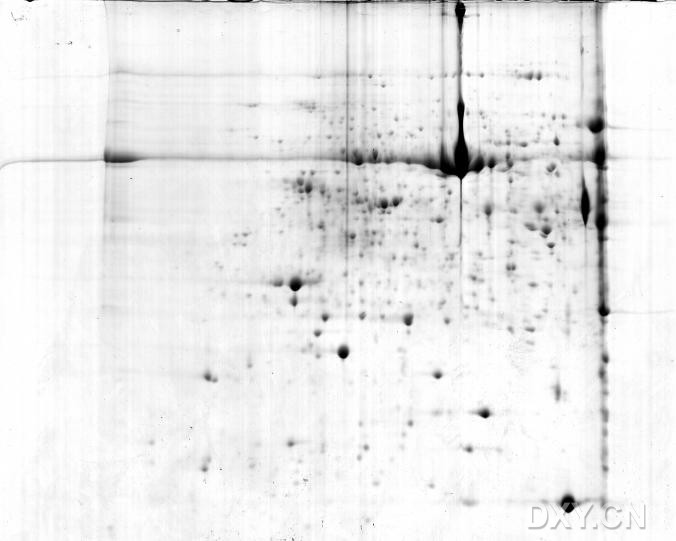
28639600.jpg



最新回复
leifengta (2014-1-24 22:13:12)
S4 grad 10,000 v 5 h
S5 step 10,000 v 40,000 vh
1/2*50000+40000=65000 还行
就是常规好像是8000v
S6 step 2000 v 8h
这一步有点不懂 维持100v 就够了吧
从图来看 有点 不要太较真了 很不错了
leifengta (2014-1-24 22:13:30)
ha111 (2014-1-24 22:14:47)
上样量 可能低了点,你这个应该是水稻叶片的电泳图谱吧,
几个高丰度的蛋白,覆盖了很多低丰度蛋白,应该设法去除那几个高丰度蛋白
superboy (2014-1-24 22:15:56)
QUOTE:
最后的S6是因为之前听GE的工程师建议说用2000v的电压去稳定聚焦比较好,他说对于18cm的胶条用100v去维持的话效果不好,所以就没有试过。。。superboy (2014-1-24 22:19:45)
QUOTE:
嗯我也觉得蛋白浓度低,但是Bradford定量出来的有8mg ml-1哦,换过BSA标线但是测几次都是那样,所以我也觉得奇怪,唉~superboy (2014-1-24 22:20:09)
QUOTE:
我的这个不是水稻的,是其他的植物,不知道那些高丰度的蛋白该怎么去除呢?跑了几次,那几个高风度蛋白在其他不同的处理中都是一直稳坐泰山滴呆在哪里,有时候还会连成一条线,看得让人难过。。。
如果上样量增加到1.2mg的话那些高丰度蛋白也会增加,怎么消除它们呢?
abc816 (2014-1-24 22:20:35)
我也在愁去除高丰度蛋白的问题,希望有经验的朋友给点建议
34723620.jpg
tuuu2 (2014-1-24 22:22:54)
具体要看是什么蛋白 然后根据性质去除 血清样品通常是IgG 160区域 有针对的除免疫球蛋白的盒子
本人不赞成这样 要保持全蛋白本身的面貌 而且不容易丢失点 或造成人为影响的嫌疑
你可以自己适当加大上样量 毕竟推荐的是根据 一块胶多少点 染色灵敏度 换算出来的 要灵活 你比我当年强多了 哈哈
xevin (2014-1-24 22:23:27)
===========================
其实这个跑蚯蚓的图已经可以了
bling (2014-1-24 22:26:23)
101010 (2014-1-24 22:27:18)
1.其实你应该做的是先使用低上样量银染进行染色,那个可以更容易看清楚聚焦程序有没有问题。目前大部分文献都是使用银染做分析胶,考染做为制备质谱的胶。
2.S6 是一个保护电压,其实你只要把S5跑完就可以了,S6的作用是在S5跑完后你不能准时的下掉第一向,此时如果不给一个电压的话,已经聚焦好的蛋白容易扩散。
3.很显然的是你的样品不适合用3-10的胶条,可以考虑换成NL 或4-7 的做做,3-10的一般都不好跑
【求助】请帮忙看看2-D图是过聚焦了还是聚焦不充分?