查看完整版本请点击这里:
分享:四大滴定的应用
1 酸碱滴定法的应用分享:四大滴定的应用
一、混合碱的测定(双指示剂法)
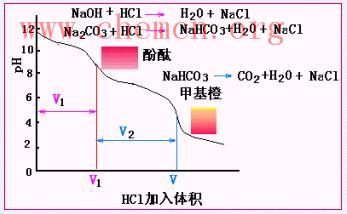
NaOH ,Na2CO3 ,NaHCO3 , 判断由哪两种组成(定性/定量计算);Na2CO3能否直接滴定, 有几个滴定突跃?以HCl为标准溶液,首先使用酚酞作指示剂,变色时,消耗HCl溶液体积V1,再加入甲基橙指示剂, 继续滴定至变色,又消耗 HCl 溶液体积V2, 如图所示:
H2CO3 = H+ + HCO3 -
pKa1 = 6.38
HCO3 - = H+ + CO32-
pKa2 = 10.25
实验结果与讨论:
(1) 当 V1>V2 时,混合碱组成:
NaOH(V1-V2) , Na2CO3 (V2)
(2) 当 V1 = V2 时,混合碱组成:Na2CO3
(3) 当 V1<V2 时,混合碱组成:
Na2CO3 (V1),NaHCO3 (V2-V1)
(4) 当 V1 = 0 时,混合碱组成: NaHCO3
(5) 当 V2 = 0 时,混合碱组成:NaOH
如何用双指示剂法测定混合酸?
二、化合物中氮含量的测定
1.蒸馏法
将铵盐试液置于蒸馏瓶中,加入过量浓 NaOH 溶液进行蒸馏,用过量的 H3BO3 溶液吸收蒸发出的 NH3:
NH3 + H3BO3 = NH4+ + H2BO3-
用HCl标准溶液滴定反应生物的 H2BO3-:
H+ + H2BO3- = H3BO3
终点时的 pH = 5 ,选用甲基红作指示剂。
2.甲醛法
6HCHO + 4NH4+ = (CH2)6N4H+ + 3H+ + 6H2O
利用 NaOH 标准溶液滴定反应生成的4个可与碱作用的H+。六次甲基四胺(CH2)6N4 是一种极弱有机碱,应选用酚酞作指示剂。
3.克氏(Kjeldahl)定氮法
氨基酸、蛋白质、生物碱中的氮常用克氏法测定。
将适量浓硫酸加入试样中加热,使 C、H 转化为 CO2 和 H2O, N元素在铜盐或汞盐催化下生成 NH4+,消化分解后的溶液中加入过量 NaOH 溶液,再用蒸馏法测定 NH3。
三、硅含量的测定
通过上述步骤,将SiO2的测定转变为HF的测定。
四、硼酸的测定
硼酸是极弱酸(pKa = 9.24)不能用标准碱直接滴定,但能与多元醇作用生成酸性较强的络合酸(pKa = 4.26),可用标准碱溶液直接滴定,化学计量点的 pH 值在9左右。用酚酞等碱性指示剂指示终点。
要点: 双指示剂法测定混合碱(混合酸)的原理、定性说明及结果计算;氨盐的测定方法及SiO2的测定方法;硼酸的测定。
[ 本帖最后由 luxuanbu 于 2010-9-13 15:00 编辑 ]
查看完整版本请点击这里:
分享:四大滴定的应用
分享:四大滴定的应用




分享:四大滴定的应用